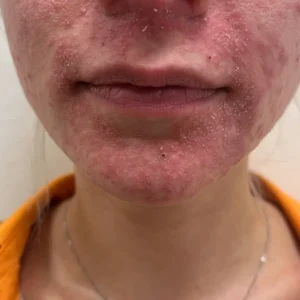
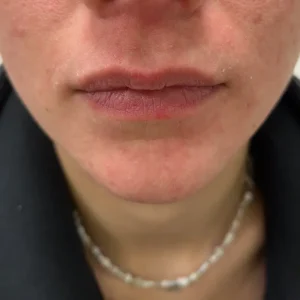
Die Kaltplasma-Therapie gehört aus meiner Sicht in jede Praxis.

Prof. Dr. med. Uwe Reinhold

Kaltplasmatherapie – innovation meets medicine
Der Quantensprung in der Dermatologie
Durch die Behandlung mit kaltem atmosphärischem Plasma werden körpereigene Regenerationsprozesse aktiviert. Reaktive Spezies regen den Zellstoffwechsel an, wodurch der insgesamte Heilungsprozess der Haut gefördert wird. Zusätzlich aktiviert Kaltplasma die Ausschüttung von Zytokinen-Proteinen, die das Zellwachstum und die Differenzierung von Zellen regulieren. * 10
Kaltplasma inaktiviert auf unkomplizierte Weise Viren, Bakterien (einschließlich multiresistenter Erreger) und Sporen. * 1,2,3,4,5,6,7,8,9
Eine Behandlung mit Kaltplasma aktiviert so, ganz ohne Resistenzen, Allergene und Nebenwirkungen, die Regeneration der Haut durch körpereigene Heilungsprozesse. Dadurch hat Kaltplasma ebenfalls einen beruhigenden Effekt auf die Haut bei z.B. Juckreiz oder Entzündungen.
Quellverweise: siehe unten
Die Kaltplasma-Therapie gehört in jede Praxis

Dr. med. Christoph Kuwert, Hamburg
Inhaber einer dermatologischen Fachpraxis mit tausenden Patienten pro Quartal
Einfacher Behandlungsablauf
Behandeln Sie effektiv, schmerzfrei und schnell
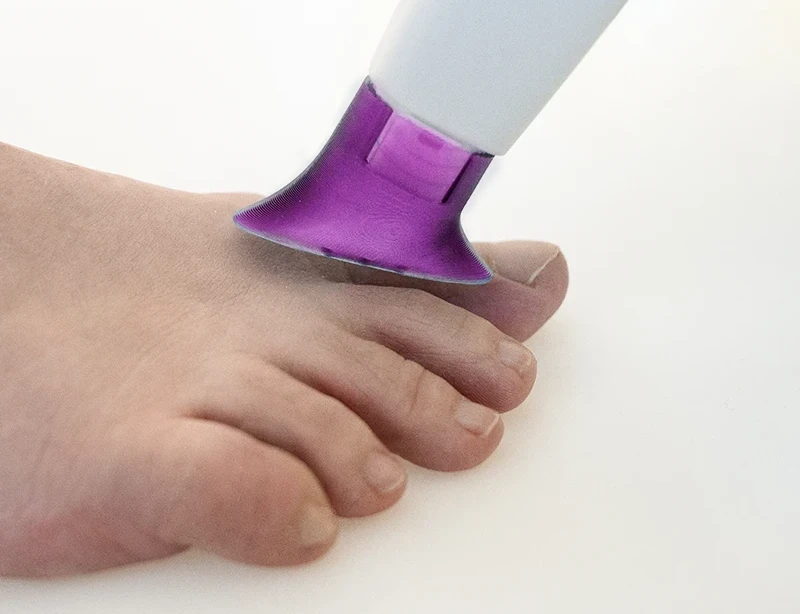
Reinigen Sie den zu behandelnden Bereich zuerst manuell. Entnehmen Sie dann das Handgerät aus der Ladeschale und bringen Sie einen sterilen Abstandhalter an. Durch einfachen Tastendruck können Sie die Anwendungsdauer auf 1 Minute oder 2 Minuten einstellen.
Halten Sie das ViroCAP® derma mit dem Abstandhalter ca. 5 mm über der zu behandelnden Fläche und starten Sie per Knopfdruck die Anwendung.
Ein akustisches Signal zeigt Ihnen jeweils nach 30 Sekunden an, dass das Gerät weitergeführt werden kann.
Ein Abstandhalter ist mit dem Start der ersten Anwendung für 20 Minuten aktiviert. Sie können also 20 Anwendungen je 1 Minute oder 10 Anwendungen je 2 Minuten am Patienten durchführen und somit auch größere Flächen problemlos behandeln.
Nach der Anwendung wird der Abstandhalter aus biokompatiblem Kunststoff entsorgt und es können bei Bedarf wirkstoffhaltige Salben oder Seren angewandt werden.
- Kein direkter Hautkontakt
- Optimale Handhabung
- Bis zu 45 Anwendungen pro Akkuladung
- Nur 128 g leicht
- Einfache Bedienung

Geplante Indikationsgebiete
- Aktinische Keratose
- Herpes Zoster
- Fußpilz
- Nagelpilz
- Dornwarzen
- Periorale Dermatitis
- Psoriasis
- Neurodermitis
- Akne vulgaris
- Rosazea
- Röschenflechte
(*) Quellangaben 1-10:
1 Arndt, S. et al. Effects of Cold Atmospheric Plasma (CAP) on ß-Defensins, Inflammatory Cytokines, and Apoptosis-Related Molecules in Keratinocytes in Vitro and in Vivo. PloS One 2015, 10 (3), e0120041. https://doi.org/10.1371/journal.pone.0120041.
2 Arndt, S. et al. Cold Atmospheric Plasma (CAP) Activates Angiogenesis-Related Molecules in Skin Keratinocytes, Fibroblasts and Endothelial Cells and Improves Wound Angiogenesis in an Autocrine and Paracrine Mode. J. Dermatol. Sci. 2018, 89 (2), 181–190. https://doi.org/10.1016/j.jdermsci.2017.11.008.
3 Arndt, S. et al. Cold Atmospheric Plasma (CAP) Changes Gene Expression of Key Molecules of the Wound Healing Machinery and Improves Wound Healing in Vitro and in Vivo. PloS One 2013, 8 (11), e79325. https://doi.org/10.1371/journal.pone.0079325.
4 Hasse, S. et al. Induction of Proliferation of Basal Epidermal Keratinocytes by Cold Atmospheric-Pressure Plasma. Clin. Exp. Dermatol. 2016, 41 (2), 202–209. https://doi.org/10.1111/ced.12735.
5 Nicol, M. J. et al. Antibacterial Effects of Low-Temperature Plasma Generated by Atmospheric-Pressure Plasma Jet Are Mediated by Reactive Oxygen Species. Sci. Rep. 2020, 10 (1), 3066. https://doi.org/10.1038/s41598-020-59652-6.
6 Hoon Park, J. et al. Comparative Study for the Inactivation of Multidrug Resistance Bacteria Using Dielectric Barrier Discharge and Nano-Second Pulsed Plasma. Sci. Rep. 2015, 5 (1), 13849. https://doi.org/10.1038/srep13849.
7 Zimmermann, J. et al. Test for Bacterial Resistance Build-up against Plasma Treatment. New J. Phys. 2012, 14 (7), 073037. https://doi.org/10.1088/1367-2630/14/7/073037.
8 Daeschlein, G. et al. Skin and Wound Decontamination of Multidrug-Resistant Bacteria by Cold Atmospheric Plasma Coagulation. J. Dtsch. Dermatol. Ges. J. Ger. Soc. Dermatol. JDDG 2015, 13 (2), 143–150. https://doi.org/10.1111/ddg.12559.
9 Bourke, P. et al. Microbiological Interactions with Cold Plasma. J. Appl. Microbiol. 2017, 123 (2), 308–324. https://doi.org/10.1111/jam.13429.
10 Weiss, Daeschlein, Kramer et. al. Virucide Properties of Cold Atmospheric Plasma for Future Clinical Applications, Journal of Medical Virology 2017, 89, 952-959.
Interesse geweckt?
Jetzt Anfragen!
Kontaktieren Sie uns unverbindlich für weitere Informationen.